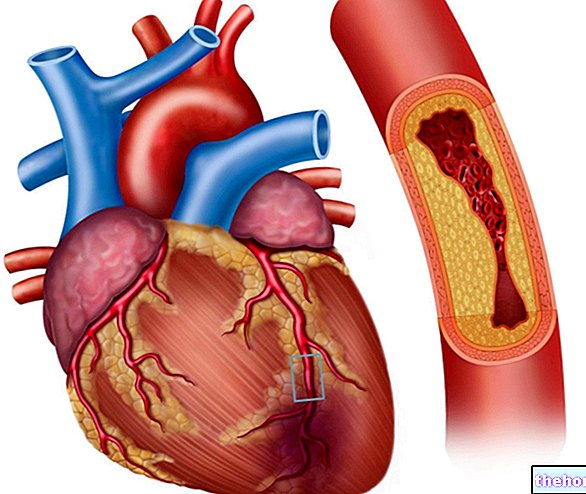
실제로 펜실베니아 대학에서 한 그룹의 연구원들은 쥐를 대상으로 한 연구에 따라 이 질병의 전형적인 뼈 파괴를 담당하는 세포 그룹을 확인했습니다.
이 발견은 인간을 대상으로 한 후속 연구에서도 확인된다면 골다공증 치료의 전환점이 될 수 있을 것이며, 이번 연구를 통해 생쥐를 대상으로 확인된 세포에 작용해 미래에 새로운 치료제가 개발될 수 있다는 가설을 세웠다. 그들의 행동을 막거나 느리게 하여 결과적으로 뼈 손실 현상을 방지합니다.
, 외상 및 골절, 특히 대퇴골, 손목, 상완골, 척추 및 발목의 위험을 증가시킵니다.여성이 가장 큰 영향을 받는다
골다공증에는 두 가지 주요 유형이 있습니다. 하나는 가장 널리 퍼져 있고 폐경기 여성이나 일반적으로 노인에게 영향을 미치는 원시적 유형이고, 다른 하나는 만성 질환을 앓고 있거나 직접적으로 약물 치료를 받고 있는 모든 연령대의 대상에게 영향을 미칠 수 있습니다. 또는 간접적으로 골격 건강에 악영향을 미칩니다.
첫 번째 유형의 경우 이탈리아에서는 50세 이상 여성 3명 중 1명(약 5,000,000명), 60세 이상 남성 8명 중 1명(약 1,000,000명)에 영향을 미치는 것으로 추산됩니다.
개발 방법
일반적으로 그리고 삶의 모든 단계에서 뼈는 생리학적 리모델링 과정을 거칩니다. 이 과정에서 오래되고 손상된 조직은 파골세포에 의해 제거되고 새로운 조직은 조골세포에 의해 재형성됩니다.
시간이 지남에 따라 파골세포의 활동이 조골세포에 비해 증가하여 자연적으로 골량의 손실이 발생합니다.
이 손실이 더 심각하고 골흡수가 형성보다 훨씬 더 커지면 골다공증이 나타납니다.
시간이 지남에 따라 변화하는 근본적인 역할을 합니다.결과는 뼈 붕괴를 결정하는 이 과정 내부의 일부 결함 메커니즘이 차례로 골다공증 발병을 유발한다는 것을 보여주었습니다.
새로운 발견 이전의 지식
이 혁신적인 발견 이전에 과학자들은 파골세포와 조골세포 사이의 균형이 건강한 뼈를 유지하는 전체 과정이 회전하는 측면을 나타낸다는 것을 이미 알고 있었습니다.
이러한 기본 지식에 직면하여, 최근까지 연구자들이 잘 알지 못했던 측면은 파골세포의 변이를 결정짓고, 파골세포가 과도하게 활동하여 뼈가 재형성되기도 전에 파괴되고, 이 과정에서 말세포로 덮인 역할은 무엇이었습니까? .
이를 이해하기 위해 작업 그룹은 2020년 3월 첫 번째 단계를 수행하여 이러한 전구체가 파골세포 형성에 필수적인 것으로 간주되는 Rankl 단백질을 생성할 수 있는 방법을 보여주었습니다.
연구의 단계
이러한 결과로부터 시작하여 Malp 세포에 Rankl 결핍이 있는 설치류에 대한 보다 심층적인 연구가 시작되었습니다.
결국, 생후 1개월이 된 설치류는 대퇴골과 같은 장골의 해면질 구성 요소에서 60~100% 범위의 밀도가 더 높은 것으로 나타났습니다. 일반적으로 마우스의 뼈 질량에 비해 매우 중요한 증가이기 때문에 중요한 발견입니다.
다음 단계에서 연구자들은 파골세포에 의해 수행되는 골흡수 기능을 조절하는 유발 인자인 말프와 이들의 분비에서 Rankl 단백질을 확인했습니다.
.
"Rankl의 분비가 비활성화될 수 있다면, 이것은 골다공증으로 고통받는 사람들의 뼈 재형성 과정의 균형을 재조정하는 데 도움이 될 수 있으며, 조골 세포가 파골 세포를 따라잡을 수 있도록 합니다."라고 Link Qin은 계속해서 치료 분야에서 가능한 발전을 위한 길을 효과적으로 열었습니다.
쥐 실험이 인간에게 옮겨져야 하고 그 타당성이 확인돼야 하기 때문에 갈 길이 멀지만, 만약 그렇다면 골다공증 분야의 치료 시나리오는 완전히 바뀔 수 있다.
실제로 결과가 확립되면 유전자 편집과 같은 일부 고급 기술을 활용하여 골 손실 과정을 차단하기 위해 세포의 행동을 조절하고 제어하는 것이 가능하다는 것이 연구자들의 희망입니다.