트립신과 키모트립신은 식품 단백질 소화의 두 가지 핵심 효소입니다. 둘 다 췌장에서 자이모겐으로, 즉 비활성 형태로 생성 및 분비됩니다. 트립신의 자이모겐 전구체는 트립시노겐이라고 하는 반면 키모트립신의 전구체는 키모트립시노겐이라고 합니다.
트립신과 키모트립신은 단백질 분해 효소(단백질 소화에 관여)의 큰 계열과 엔도펩티다아제의 하위 그룹에 속합니다. 위 펩신 및 췌장 엘라스타제를 포함한 이러한 물질은 아미노산 사슬 내의 펩티드 결합을 공격하여 더 작은 분자 단편을 생성합니다. exopeptidase의 두 번째 그룹에 속하는 효소는 트립신과 키모트립신의 작업을 완료하여 펩티드 사슬의 끝에서 단일 아미노산을 분리합니다. 췌장의 카르복시펩티다아제(A1, A2 및 B, 카르복실 말단을 공격함)뿐만 아니라 소장 점막에서 생성 및 분비되는 아미노펩티다아제(아미노 말단 말단을 공격함) 및 디펩티다아제도 이 패밀리에 속합니다. 트립신(트립시노겐) 및 키모트립신(키모트립시노겐)에서 볼 수 있는 것과 유사하게 췌장에서 비활성 형태로 분비됩니다. 세 가지 경우 모두 효소 활성화 과정에 관여하는 효소는 세포에서 생성 및 분비되는 단백질인 엔테로펩티다제입니다 더 구체적으로, enteropeptidase는 트립시노겐에 특이적이며 트립신으로 전환되면 동일한 트립시노겐을 비롯한 다른 단백질 분해 효소도 활성화됩니다.
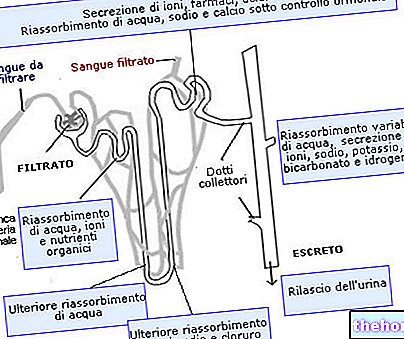
십이지장은 소장의 첫 번째 부분이며 췌장액이 유입될 뿐만 아니라 pH 보정과 지질 소화에 필수적인 간액(담즙)도 흐른다는 점을 간단히 기억합시다.

트립신과 키모트립신의 기능적 차이점은 단순히 특정 아미노산에 의해 형성된 결합만을 인식하고 분할하는 능력인 특이성과 관련이 있습니다. 트립신은 무엇보다도 염기성 아미노산(예: 아르기닌 및 라이신)과 결합하는 펩티드 결합에 작용하는 반면 키모트립신은 주로 티로신, 페닐알라닌, 트립토판, 류신 및 메티오닌과 관련된 결합을 가수분해합니다.
다양한 단백질 분해 효소 덕분에 위산의 영향을 받아 원래 수십 개의 아미노산으로 구성된 식단의 단백질이 디펩티드, 트리펩티드 및 유리 아미노산으로 분해되며, 모두 쉽게 흡수될 수 있는 물질인 모세혈관에서 유래합니다. 간으로 운반되는 장 점막.
대변의 트립신과 키모트립신
대변에서 키모트립신과 트립신의 측정은 외분비 췌장의 기능적 능력에 대한 간접적인 테스트로서 과거에는 특히 그러했습니다. 이 샘 수준의 무언가가 제대로 기능하지 않으면 대변에서도 결핍될 트립신과 키모트립신 합성 감소를 예상하는 것이 논리적입니다. 테스트는 감도가 좋지만 위양성 및 위음성의 실제 위험이 있습니다. 예를 들어, 완하제의 사용은 대변의 효소 농도를 감소시키는 반면 췌장 소화 추출물(예: 판크레아틴) 또는 야채(예: 파인애플 줄기, 파파야, 파파인 및 브로멜라인)의 섭취는 위음성 결과를 유발합니다. 장내 세균총은 또한 변에 변화 없이 도착하는 트립신과 키모트립신의 양에 약간의 영향을 미치므로 항생제 사용은 위음성을 유발할 수 있습니다. 반대로 게실증 및 세균 증식을 선호하는 기타 조건이 있는 경우 위양성 결과가 기록될 수 있습니다.
대변에 대한 트립신 및 키모트립신 분석의 고전적인 적용은 낭포성 섬유증 환자의 췌장 기능 부전을 감지하는 것입니다.이 질병의 결과 중 하나는 췌장에서 십이지장으로 트립신 및 기타 소화 효소의 정상적인 수송 손상입니다. ; 이 때문에 낭포성 섬유증이 있는 아이는 태어날 때 대변이 특히 조밀하여 장폐색을 일으키기 때문에 태변에 특히 적은 양의 키모트립신과 트립신이 존재합니다.