리탁이란?
Litak은 활성 물질 cladribine을 포함하는 주사용 용액입니다.
Litak은 무엇에 사용됩니까?
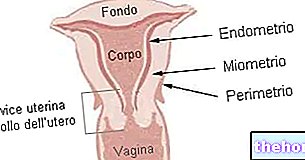
Litak은 "B 림프구(백혈구의 일종)의 과잉 생산으로 인한 혈액암"인 털이 많은 세포 백혈병 성인을 치료하는 데 사용됩니다. "유모 세포"라는 용어는 머리카락처럼 보이는 돌기를 말합니다. 현미경으로 관찰할 수 있습니다. 림프구의 표면.
털이 많은 백혈병 환자가 적어 희귀질환으로 분류돼 2001년 9월 18일 리탁이 희귀의약품(희귀질환 치료제)으로 지정됐다.
약은 처방전이 있어야만 구할 수 있습니다.
Litak은 어떻게 사용됩니까?
Litak 치료는 암 치료 경험이 있는 의사가 시작해야 합니다. Litak은 피하 주사로 투여됩니다. 권장 용량은 체중 1kg당 0.14mg이며 5일 동안 하루에 한 번 복용합니다. 환자는 적절한 훈련을 통해 스스로 주사할 수 있습니다. Litak은 중등도에서 중증의 간 또는 신장 문제가 있는 환자에게 투여해서는 안 됩니다. 65세 이상의 환자에서는 주의해서 사용해야 하며 간, 신장 및 혈구 수를 자주 검사해야 합니다. .
Litak은 어떻게 작동합니까?
Litak의 활성 물질인 Cladribine은 "항대사제"라고 불리는 항암제의 종류에 속하는 암세포와 같은 분열 세포를 죽일 수 있는 약물인 세포독성 약물입니다. 클라드리빈은 퓨린(화학 구조가 퓨린과 유사한 물질)의 "유사체"입니다. 퓨린은 DNA를 구성하는 기본 화학 물질 중 하나입니다. 체내에서 클라드리빈은 림프구에서 화학 물질인 CdATP로 전환되어 새로운 DNA 생성에 관여합니다. 이것은 세포 분열을 방지하여 백혈병의 진행을 늦춥니다. CdATP는 또한 다른 세포, 특히 다른 혈액 세포에 영향을 미칠 수 있습니다. 클라드리빈은 1980년대부터 항암제에 사용되어 왔으며 1993년부터 유럽 연합(EU)의 일부 회원국에서 정맥 주입(정맥 내 점적)으로 이용 가능했습니다.
Litak은 어떻게 연구되었습니까?
클라드리빈은 수년 동안 사용되어 왔기 때문에 이미 의학 문헌에 발표된 데이터를 제시했습니다. 63명의 성인 모발 세포 백혈병을 대상으로 한 주요 연구에서 Litak이 연구되었습니다.이 연구에서 Litak은 다른 치료법과 비교되지 않았습니다.효과의 주요 척도는 치료 후 완전 또는 부분 관해를 보인 환자의 수였습니다. 완전관해는 질병의 징후가 사라지는 것을 의미하고, 부분관해는 혈구수 개선 및 암세포 수 감소를 의미합니다.
연구 기간 동안 Litak이 보여준 이점은 무엇입니까?
주요 연구에서 환자의 97%가 완전 또는 부분 관해(62명 중 60명)를 보였고 76%가 완전 관해(62명 중 47명)를 보였습니다. 이러한 결과는 정맥 내 클라드리빈 사용에 대한 다른 발표된 연구에서 발견된 것과 유사하고 인터페론 알파 및 펜토스타틴과 같은 대체 치료법으로 얻은 결과보다 우수합니다.
Litak과 관련된 위험은 무엇입니까?
Litak과 관련된 가장 흔한 부작용(환자 10명 중 1명 이상에서 나타남)은 감염, 범혈구 감소증 또는 골수 억제(낮은 혈구 수), 자반병(피부 병변), 면역 억제(면역 체계 약화), 혈압 감소입니다. 식욕부진, 두통, 현기증, 호흡이상 및 흉음, 기침, 메스꺼움, 구토, 변비, 설사, 발진, 국소발진(발진), 발한(과도한 발한), 주사부위 반응(주사부위의 통증 및 염증), 발열 , 피로, 오한 및 무력감(약점) Litak에 보고된 전체 부작용 목록은 패키지 전단지를 참조하십시오.
Litak은 클라드리빈 또는 기타 성분에 과민증(알레르기)이 있을 수 있는 환자에게 사용해서는 안 됩니다. Litak은 임신 또는 모유 수유 중, 18세 미만의 환자, 중등도에서 중증의 신장 또는 간 질환 환자, 또는 혈구 생성을 감소시키는 다른 약물과 함께 사용해서는 안 됩니다.
Litak이 승인된 이유는 무엇입니까?
인체용 의약품 위원회(CHMP)는 Litak의 이점이 모세포 백혈병 치료에 대한 위험보다 더 크다고 결정했습니다. 위원회는 Litak에 대한 판매 허가 승인을 권고했습니다.
리탁에 대해 더 알아보기
2004년 4월 14일 유럽 위원회는 Litak에 대해 Litak에 대한 "판매 허가"를 유럽 연합 전역에서 유효하게 승인했으며, "판매 허가"는 2009년 4월 14일에 갱신되었습니다.
Litak 희귀의약품 위원회의 의견 요약을 보려면 여기를 클릭하십시오.
Litak EPAR의 전체 버전을 보려면 여기를 클릭하십시오.
이 요약의 마지막 업데이트: 2009년 4월 4일.
이 페이지에 게시된 Litak - cladribine에 대한 정보는 오래되었거나 불완전할 수 있습니다. 이 정보를 올바르게 사용하려면 고지 사항 및 유용한 정보 페이지를 참조하십시오.