" 첫 번째 부분
크렙스 회로의 네 번째 단계를 촉매하는 효소는 α-케토글루타레이트 탈수소효소; 이 효소는 피루브산 탈수소효소와 매우 유사한 효소 복합체입니다. 둘 다 48-60개의 단백질로 구성되어 있으며 3가지 다른 효소 활성이 인식되고 동일한 효소 보조 인자를 가지고 있습니다. 피루브산과 피루브산 모두 유사한 기질에 작용하기 때문에 매우 유사한 효소입니다.α-케토 글루타레이트는 α- 케토산. 두 효소 복합체의 작용 메커니즘은 동일합니다.
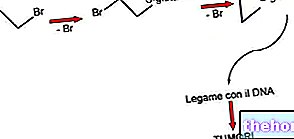
티아민 피로포스페이트가 카르보닐(C = O)에 대한 공격 "α-ketoglutarate는 탈카르복실화를 일으키고 카르복시하이드록시 프로필 유도체가 형성됩니다. 리포아미드로의 후속 이동으로 내부 산화환원 과정이 발생하여 리포아미드 카르복시-유도체 또는 숙시닐 리포아미드를 얻습니다.
그런 다음 석시닐 리포아미드는 조효소 A와 반응하여 석시닐 조효소 A(크렙스 회로에서 계속됨)와 FAD에 의해 재산화되는 환원된 리포아미드를 제공합니다. 형성된 FADH2는 NAD+에 의해 재산화되고 NADH가 얻어집니다. 따라서 이 단계에서 이산화탄소의 형태로 탄소질 골격에서 탄소가 두 번째로 제거됩니다.
조효소 A에 연결된 아실기는 활성화된 형태, 즉 에너지 함량이 높기 때문에 숙시닐 조효소 A의 에너지를 이용할 수 있습니다.

크렙스 회로의 다섯 번째 단계에서 숙시닐 조효소 A는 숙시닐 티오키나아제; 그것의 작용 방식에 대해 두 가지 가설이 세워졌습니다. 우리는 그것이 가장 공인된 것이기 때문에 둘 중 하나만 설명할 것입니다. 이 가설에 따르면, 숙시닐 조효소 A는 효소의 히스티딘(Hys)의 질소에 의해 공격을 받는다: 조효소 A가 방출되고 히스티딘으로부터 유도된 부가물이 중간체로서 형성된다, 즉 숙시닐-효소(또는 숙시닐-Hys) ); 오르토인산은 이 중간체에 작용하여 숙시네이트의 방출과 인효소의 형성을 유도합니다. 인효소는 구아노신 이인산(GDP)의 공격을 받아 구아노신 삼인산(GTP)을 생성하고 효소가 방출됩니다. 에너지 관점에서 GTP = ATP: 에너지를 제공하는 결합은 두 종 모두에서 동일합니다(포스포릴 Β와 포스포릴 γ 사이의 무수물 결합). 어떤 경우에는 GTP를 에너지 함량이 높은 물질로 사용하기도 하지만 일반적으로 GTP는 효소의 작용에 의해 ATP로 전환된다. 뉴클레오사이드 디포스포 키나제 (NDPK); 세포에서 발견되는 효소이며 다음 반응을 촉매합니다.
N1TP + N2DP → N1DP + N2TP
일반 NiTP ® 뉴클레오사이드 삼인산
일반 NiDP ® 뉴클레오시드 이인산
가역적인 반응입니다. 우리의 경우 다음과 같은 일이 발생합니다.
GTP + ADP → GDP + ATP
따라서 시약 농도의 작은 변화에도 오른쪽이나 왼쪽으로 진행할 수 있습니다.
크렙스 주기가 에너지 요구량보다 높은 ATP 생성을 유도하는 속도로 진행되면 ATP는 많이 있는 반면 ADP는 거의 사용할 수 없습니다. 뉴클레오사이드 디포스포 키나제에 의해 촉매되는 반응은 다음과 같습니다. 왼쪽으로 향함(뉴클레오시드 디포스포 키나제가 충분한 기질, 즉 ADP를 갖지 않는 경우 GTP가 축적됨). 따라서 GTP는 에너지 가용성의 신호이므로 크렙스 주기를 늦춥니다.
크렙스 회로의 여섯 번째 단계는 다음 작용에 의해 푸마르산염이 형성됩니다. 숙시네이트 탈수소효소; 이 효소는 불포화(알켄) 트랜스, 즉 푸마르산염(시스 이성질체가 말레산염인 동안)이 항상 형성되기 때문에 입체특이 반응을 나타냅니다. 석시네이트 탈수소효소는 미토콘드리아 내부 막에서 발견되는 반면 크렙스 회로의 다른 모든 효소는 미토콘드리아 전체에 흩어져 있습니다.
숙시네이트 탈수소효소는 보조인자로 FAD를 가지고 있습니다. oxaloacetate(피드백 억제)에 의해 억제되는 반면, succinate와 fumarate는 positive modulator(activator)로 사용됩니다. 크렙스 주기는 에너지를 필요로 하므로 환자로부터 옥살로아세테이트를 얻을 수 있는 유일한 가능성은 환자의 농도가 매우 높다는 것입니다. oxaloacetate의 농도는 citrate synthase의 작용에 의해 낮게 유지된다는 사실.숙신산 탈수소효소에 의해 촉매되는 반응은 자가 공급 반응이며 이것이 말산을 옥살로아세테이트로 전환시키는 유일한 방법입니다.
미토콘드리아 말산염의 농도는 세포질 말산염의 농도와 양립할 수 있어야 합니다. 미토콘드리아 말산염의 농도가 말산염의 옥살로아세테이트로의 전환을 보장할 정도로 높을 때만(크렙스 회로에서) 말산염은 다음에도 사용할 수 있습니다. 다른 방법(세포질): 세포질에서 말산염은 GOT(아미노전이효소) 또는 포도당 신생합성을 통해 포도당의 작용에 의해 아스파테이트를 얻을 수 있는 옥살로아세트산으로 전환될 수 있습니다.
우리는 효소에 의해 촉매되는 크렙스 주기의 일곱 번째 단계로 돌아갑니다. 푸마라시: 물을 입체적으로 첨가하여 L-말레이트를 만듭니다.
우리가 이미 말한 Krebs 주기의 마지막 단계에서, 말산 탈수소효소. 이 효소는 촉매 작용을 위해 NAD + 분자를 사용합니다.
따라서 우리는 크렙스 주기의 다양한 단계에 대한 설명을 마쳤습니다.
크렙스 주기는 완전히 가역적입니다.
크렙스 주기의 속도를 높이려면 해당 주기에 존재하는 대사 산물의 농도를 높일 수 있습니다. 크렙스 회로의 속도를 높이는 전략 중 하나는 미토콘드리아로 들어가는 피루브산의 일부를 옥살로아세테이트로 전환하고(피루브산 카르복실라제의 작용에 의해) 모든 것을 아세틸 조효소 A로 전환하지 않는 것입니다. 따라서 옥살로아세테이트의 농도를 증가시킵니다. 크렙스 주기의 대사 산물이므로 전체 주기의 속도를 증가시킵니다.
크렙스 주기에서 3개의 NAD+는 3개의 NADH로, 하나의 FAD는 FADH2로 변환되며, 또한 GTP가 획득됩니다. 크렙스 주기에서 얻은 환원력을 전달하여 추가 ATP가 생성됩니다. 호흡 사슬에서 환원력은 NADH와 FADH2에서 산소로 전달됩니다. 이 전달은 미토콘드리아 막에 위치한 일련의 효소에 기인합니다. 이 효소는 작용하여 ATP를 생성합니다.
호흡 사슬의 과정은 exergonic 과정이며 유리된 에너지는 ATP를 생성하는 데 사용됩니다. 호흡 사슬에 들어가는 각 NADH 분자에 대해 2.5 분자의 ATP가 얻어지고 각 FADH2에 대해 1.5 분자의 ATP가 얻어집니다. 이 다양성은 FADH2가 NADH보다 낮은 수준에서 호흡 사슬에 들어간다는 사실 때문입니다.
호기성 대사의 환원력으로 약 33%의 효율로 30-32 ATP(219-233kcal/mol)를 얻습니다(무산소 대사의 효율은 약 2%).