
톨루라란?
Tolura는 활성 물질 telmisartan을 포함하는 약입니다. 흰색 정제(원형: 20mg, 타원형: 40mg, 캡슐형: 80mg)로 제공됩니다.
톨루라는 '제네릭 의약품'입니다. 이는 유럽연합(EU)에서 이미 승인된 미카디스라는 '대조약'과 유사하다는 의미다.
Tolura는 무엇에 사용됩니까?
톨루라는 성인의 본태성 고혈압(고혈압) 치료제로, "본태성"이라는 용어는 고혈압이 명백한 원인이 없음을 의미합니다.
약은 처방전이 있어야만 구할 수 있습니다.
Tolura는 어떻게 사용됩니까?
Tolura의 권장 용량은 1일 1회 40mg이지만 일부 환자는 20mg 용량을 사용하여 이점을 찾을 수 있습니다. 원하는 혈압에 도달하지 못한 경우 최대 80mg까지 증량하거나 히드로클로로치아자이드와 같은 다른 고혈압 치료제를 추가할 수 있습니다.
Tolura는 어떻게 작동합니까?
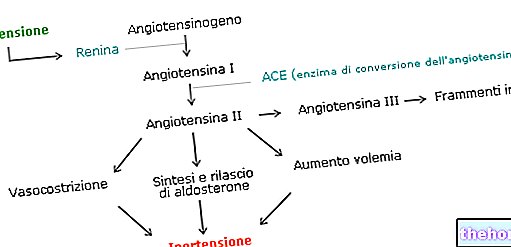
톨루라의 활성물질인 텔미사르탄은 '안지오텐신 II 수용체 길항제'로 체내에서 생성되는 안지오텐신 II라는 호르몬의 작용을 차단한다는 의미이며, 안지오텐신 II는 강력한 혈관수축제(혈관을 제한하는 물질)입니다. 텔미사르탄은 지오텐신 II가 정상적으로 부착하는 수용체를 차단함으로써 혈관이 확장되도록 하여 호르몬의 작용을 방지하여 혈압을 낮추고 심장마비나 뇌졸중과 같은 고혈압과 관련된 위험을 줄입니다.
Tolura는 어떻게 연구되었습니까?
Tolura는 제네릭 의약품이기 때문에 연구는 해당 의약품이 참조 의약품인 Micardis와 생물학적으로 동등하다는 것을 보여주도록 설계된 증거로 제한되었습니다. 두 의약품은 체내에서 동일한 수준의 활성 물질을 생성할 때 생물학적으로 동등합니다.
Tolura의 이점과 위험은 무엇입니까?
Tolura는 제네릭 의약품이며 대조약과 생물학적으로 동등하기 때문에 해당 약의 이점과 위험은 대조약과 동일하다고 가정합니다.
Tolura가 승인된 이유는 무엇입니까?
CHMP(Committeee for Medicinal Products for Human Use)는 EU 요구 사항에 따라 Tolura가 Micardis와 비슷한 품질과 생물학적 동등성을 갖는 것으로 나타났다고 결론지었습니다. Micardis의 경우 이익이 확인된 위험보다 더 큽니다.따라서 위원회는 Tolura에 대한 판매 허가를 승인할 것을 권고했습니다.
톨루라에 대한 추가 정보
2010년 6월 4일, 유럽연합 집행위원회는 유럽 연합 전역에서 유효한 Tolura에 대한 "판매 허가"를 Krka dd, Novo Mesto에 발행했습니다. "판매 허가"는 5년 동안 유효하며 그 후 갱신할 수 있습니다.
Tolura EPAR의 전체 버전을 보려면 여기를 클릭하십시오. Tolura 요법에 대한 자세한 내용은 패키지 전단지(EPAR에도 포함됨)를 읽거나 의사나 약사에게 문의하십시오.
참조 의약품의 전체 EPAR 버전은 FDA 웹사이트에서도 찾을 수 있습니다.
이 요약의 마지막 업데이트: 2010년 4월 4일.
이 페이지에 게시된 Tolura에 대한 정보는 최신 정보가 아니거나 불완전할 수 있습니다. 이 정보를 올바르게 사용하려면 고지 사항 및 유용한 정보 페이지를 참조하십시오.








.jpg)














.jpg)


