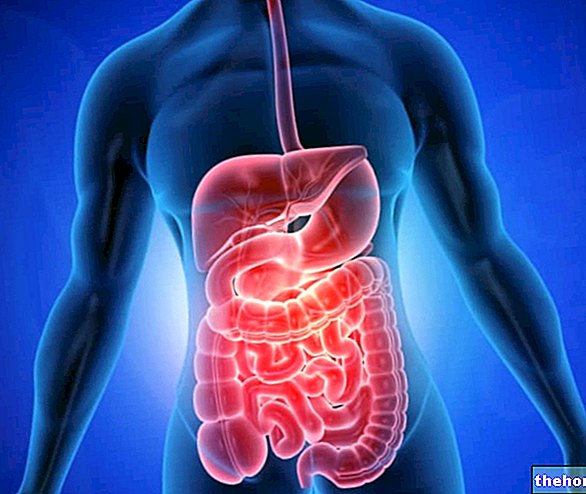
프로테아제(또는 펩티다제): 단백질 소화에 관여하는 가수분해 효소. 이 작용으로 프로테아제는 다양한 아미노산을 결합하고 단백질 분자가 반복적으로 연결되는 펩티드 결합을 끊을 수 있습니다.

기원
- 펩신: 비활성 형태(펩시노겐)로 위장의 소화 세포에서 생성됩니다. 염산에 의해 활성화되며 주로 방향족 아미노산(예: 티로신, 트립토판 및 페닐알라닌)과 결합하는 펩타이드 결합에 개입합니다.
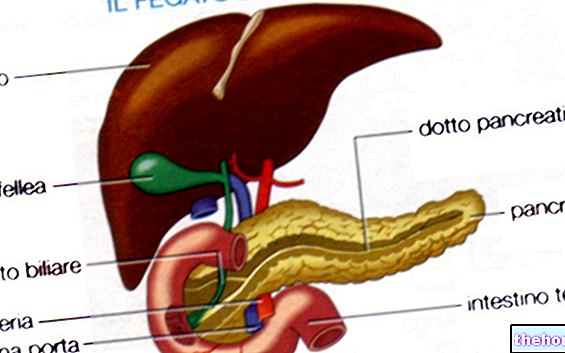
- 트립신: 비활성 형태(트립시노겐)로 외분비 췌장에서 생성됩니다. 십이지장 엔테로펩티다아제에 의해 활성화되며, 주로 염기성 아미노산(아르기닌 및 라이신 등)과 결합하는 펩티드 결합에 개입합니다.
- 키모트립신: 비활성 형태로 외분비 췌장에서 생성됩니다(키모트립시노겐). 트립신에 의해 활성화됩니다. 주로 방향족 아미노산(예: 티로신, 트립토판 및 페닐알라닌)과 결합하는 펩티드 결합에 개입합니다.
- Elastase: 비활성 형태로 외분비 췌장에서 생성됩니다(pre-pro-elastase). 트립신에 의해 활성화됩니다. 엘라스틴을 공격할 수 있는 유일한 효소로서 육류 식품의 소화에 매우 중요합니다.
- Carboxypeptidase: 부분적으로는 활성 형태로, 부분적으로는 비활성 형태로 외분비 췌장에서 생성 및 분비됩니다. 그들은 아미노산 사슬의 카르복실 말단에 위치한 펩타이드 결합에 개입합니다.
- 아미노펩티다아제: 십이지장 점막에서 생성되고 분비됩니다. 그들은 아미노산 사슬의 카르복실 말단에 위치한 펩타이드 결합에 개입합니다.
- 디펩티다아제: 소장의 장세포에서 분비되며, 한 쌍의 아미노산을 결합하는 펩티드 결합을 가수분해합니다.
식품 매개 단백질의 소화에 사용되는 프로테아제는 그들이 속한 대과의 작은 부분에 불과합니다. 많은 호르몬과 마찬가지로 효소가 단백질 성질의 분자라고 생각하면 프로테아제의 역할이 얼마나 중요한지 깨닫게 됩니다. 필요한 경우 특정 프로테아제를 사용하여 분자를 분해하는 것보다 이러한 분자의 활성을 조절하는 더 좋은 방법은 무엇입니까? 여기에서 면역 체계의 세포에는 외부 미생물의 세포막을 소화하는 단백질 분해 효소가 포함되어 있으며, 이 단백질 분해 효소는 한편으로는 단백질 분해 효소를 분비하여 세포를 침범하는 능력을 가지고 있고 다른 한편으로는 우리가 스스로를 방어해야 하는 단백질 독소(외독소)를 방출하기 위해 안티트롬빈 III 및 플라스민과 같은 일부 혈장 프로테아제는 응고에 중요한 역할을 하여 "대신 트롬빈에 의해 강화되는 이 메커니즘의 과도한 활성화를 방지합니다. 프로테아제의 대가족).
따라서 프로테아제의 조절 작용은 다양한 신체 기능의 조절에 기본적이며, 예를 들어 비정상적인 단백질이 단백질 합성에서 비롯된 경우 가능한 한 빨리 분해되는 것이 매우 중요합니다. 무한대로 성장하지만 특정 프로테아제에 의해 제한되어야 합니다. 게다가 프로테아제가 단백질 분자를 분해하고 파괴한다고 생각한다면 다른 프로테아제를 포함하여 그 기능을 조절하여 고양된 단백질 분해 현상을 방지할 수 있는 요인이 있을 것으로 예상해야 합니다. 결국 유기체의 조직에 손상을 입힙니다.
근육 섬유에 영향을 미치는 단백질 분해 현상은 일부 포도당 생성 아미노산에서 시작하여 에너지와 포도당을 생성하기 위해 단식 및 장기간의 신체 운동에 의해 활성화됩니다.
식물 프로테아제는 또한 병원체를 방어하고 펩티드를 분해하며 다른 단백질의 구조와 기능을 수정하기 위해 식물에 의해 합성됩니다. 파인애플 줄기(브로멜라인), 파파야(파파인) 및 싹이 튼 씨앗(보리 맥아)이 특히 풍부합니다. 이러한 식품 또는 그 추출물을 섭취하면 소화관에서 방출되는 내인성 프로테아제의 작용을 도와 소화 기능을 조절하는 데 도움이 됩니다.